칸디다증은 곰팡이균 칸디다(Candida)가 혈액을 통해 전신으로 퍼지며 장기 손상과 패혈증을 유발하는 치명적인 감염질환이다. 최근 면역저하 치료, 장기이식, 의료기기 사용 증가로 칸디다증이 급증하고 있다.
현재 사용 중인 칸디다 항진균제들은 표적 선택성이 낮아 인체 세포에도 영향을 미칠 수 있고, 내성을 갖는 새로운 균의 출현으로 치료 효과도 점차 떨어지고 있다.
특히 면역력이 저하된 환자는 감염 진행이 빠르고 예후도 좋지 않아 기존 치료제의 한계를 극복할 수 있는 새로운 치료법 개발이 시급하다.
내성 극복 칸디다증 치료제
KAIST 생명과학과 정현정 교수팀이 기존 항진균제와 달리 칸디다균에만 선택적으로 작용해 높은 치료 효능과 낮은 부작용을 동시에 갖춘 차세대 치료제 개발에 성공했다고 8일 밝혔다.
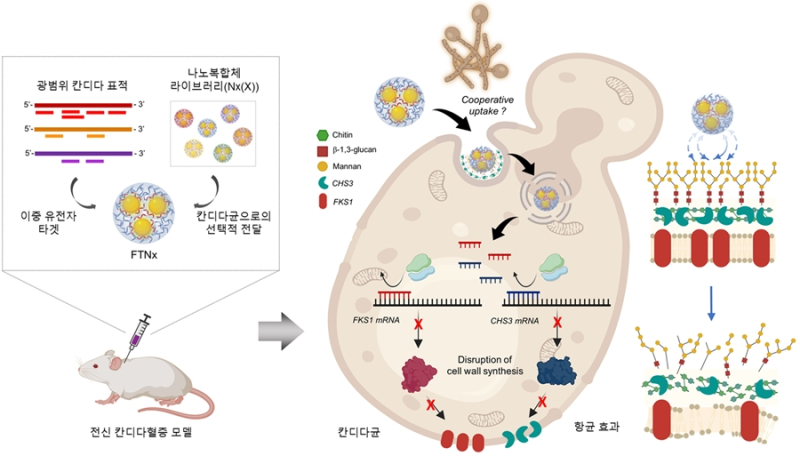
정 교수팀은 서울아산병원 정용필 교수팀과 협력해 칸디다 세포벽의 두 핵심 효소를 동시에 저해하는 유전자 기반 나노치료제(FTNx)를 개발했다.
이 치료제는 전신 투여가 가능하고 유전자 억제기술과 나노소재 기술을 융합함으로써 기존 화합물 기반 약물이 가지는 구조적 한계를 효과적으로 극복, 칸디다균에만 선택적으로 치료할 수 있다.
연구팀은 칸디다라는 곰팡이균의 세포벽을 만드는 데 중요한 β‑1,3‑글루칸 합성효소(FKS1)와 키틴 합성효소(CHS3)를 동시에 표적하는 짧은 DNA 조각(ASO)을 탑재한 금나노입자 기반 복합체를 제작했다.
여기에 칸디다 세포벽의 특정 당지질 구조와 결합하는 표면 코팅기술을 적용해 표적유도장치를 장착함으로써 인체 세포에는 아예 전달되지 않고 칸디다에만 선택적으로 작용하는 정밀 타겟팅 효과를 구현했다.
이 복합체는 칸디다 세포 내로 진입한 후 FKS1 및 CHS3 유전자가 만들어내는 mRNA를 잘라버려 번역을 억제, 세포벽 성분인 β‑1,3‑글루칸과 키틴의 합성을 동시에 차단한다.
이로 인해 칸디다 세포벽은 구조적 안정성을 유지하지 못하고 붕괴, 세균의 생존과 증식이 억제된다.
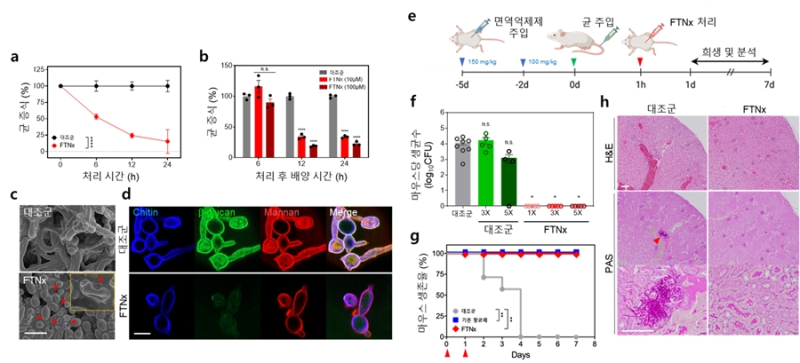
실제 전신 칸디다증 쥐 모델 실험에서 칸디다의 장기 내 균 감소, 면역 반응 정상화, 생존율 증가 등을 확인했다.
정현정 교수는 “이번 연구는 기존 치료제가 인체 독성과 약제내성 확산 문제를 극복하는 방법을 제시하며 유전자 치료의 전신 감염 적용 가능성을 보인 중요한 전환점”이라며 “향후 임상적용을 위한 투여방식 최적화 및 독성 검증연구를 지속 진행할 계획”이라고 밝혔다.
한편, 이번 연구는 KAIST 생명과학과 정주연 석박사통합과정과 서울아산병원 홍윤경 박사가 제1저자로 수행했고, 연구결과는 국제학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 지난 1일자에 게재됐다.
(논문명 : Effective treatment of systemic candidiasis by synergistic targeting of cell wall synthesis / DOI : 10.1038/s41467-025-60684-7)