한미약품이 한국인에게 최적화된 GLP-1 비만치료제의 상용화를 위한 마지막 임상에 돌입한다.
한미약품은 자체 개발한 GLP-1 수용체 작용제 계열 약물인 ‘에페글레나타이드’의 임상 3상 계획에 대한 식품의약품안전처 승인을 23일 획득했다고 밝혔다.
에페글레나타이드는 체내에서 인슐린 분비와 식욕 억제를 돕는 GLP-1 호르몬의 유사체로 작용한다. 한미약품의 독자 플랫폼 기술 ‘랩스커버리’가 적용된 주 1회 제형 GLP-1 제제로, 과거 파트너사였던 사노피가 진행한 다수의 글로벌 임상을 통해 약물의 혁신성을 입증 받은 바 있다.
앞서 한미약품은 식품의약품안전처 글로벌 혁신제품 신속심사 지원체계의 1대1 협의체 밀착 지원을 받아 바이오의약품 개발 전략을 수립하고, 제품화 컨설팅을 위해 ‘유전자 재조합 의약품 맞춤형 상담 프로그램’을 진행했다. 이를 통해 에페글레나타이드 임상 및 허가 전략에 대한 규제 당국과의 긴밀한 소통 기회를 확보했으며, 예상되는 난제 중 상당 부분을 사전에 해소할 수 있었다.
지난 2015년 글로벌 제약기업 사노피에 라이선스 아웃된 이후 진행한 대규모 글로벌 임상 3상에서 체중 감소와 혈당 조절 효력을 확인했으며, 주요 심혈관계 및 신장 질환 발생률을 유의미하게 감소시켜 세계적 권위 학술지인 뉴잉글랜드 저널 오브 메디슨(NEJM) 등 학술지에 해당 결과가 등재되기도 했다.
한미약품은 에페글레나타이드의 혁신적 잠재력이 글로벌 대규모 임상으로 확인된 만큼, 3년 내 국내에서 상용화할 수 있도록 속도감 있게 임상 개발을 진행할 방침이다.
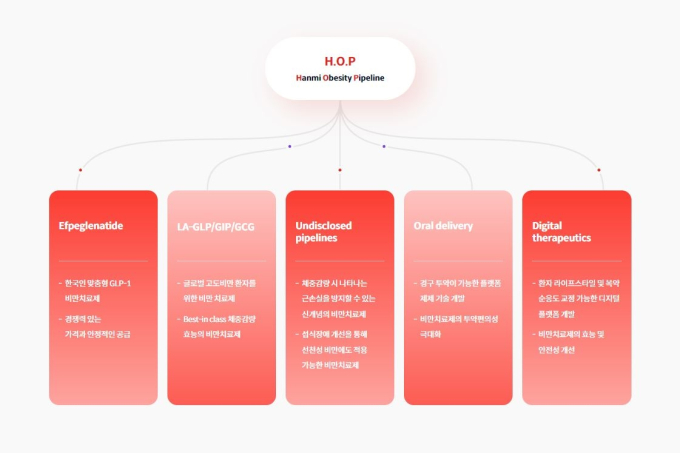
김나영 한미약품 전무는 “비만도 치료가 필요한 만성질환이라는 인식이 세계적으로 확산하고 있다”며 “처음부터 끝까지 독자 기술로 개발한 최초의 GLP-1 비만 신약을 시작으로 한미 비만 프로젝트(H.O.P) 개발을 통해 혁신적 성과를 창출할 수 있도록 최선을 다하겠다”고 말했다.
한편, 글로벌 비만치료제 시장은 2021년 32억달러(한화 약 4조2900억원)에서 2026년 46억달러(약 6조1700억원) 규모로 성장할 것으로 전망된다.



































