유한양행의 ‘렉라자’(성분명 레이저티닙)와 다국적 제약사 얀센의 ‘리브리반트’(성분명 아미반타맙) 항암제 병용요법이 기존 3세대 표적 치료제보다 우수한 치료 효과를 보였다는 연구 결과가 나왔다.
조병철 연세암병원 폐암센터장 연구팀은 표피 성장인자 수용체(EGFR) 돌연변이 폐암 환자를 대상으로 진행한 다국가, 무작위 배정 3상 연구에서 아미반타맙·레이저티닙 병용 요법이 기존 표준치료제 ‘오시머티닙’(상품명 타그리소)보다 무진행생존기간을 30% 정도 높였다고 1일 밝혔다. 아미반타맙과 레이저티닙은 각각 진행성 EGFR 돌연변이 폐암, EGFR 엑손20 돌연변이 폐암 약제로 식품의약품안전처의 승인을 받았다.
이번 임상 결과는 국제학술지 ‘뉴잉글랜드 저널 오브 메디신’(New England Journal of Medicine, IF 176.082)에 실렸다. 국산 항암제 임상 결과가 해당 학술지에 게재된 것은 이번이 처음이다.
EGFR 돌연변이 폐암은 전체 폐암 중 25~40%를 차지하며, 전 세계적으로 매년 45만명의 신규 환자가 발생한다. 현재 1차 치료제로 미국 식품의약국(FDA) 승인을 받은 약제는 오시머티닙이 유일하다. 오시머티닙은 반응률 80%와 무진행생존기간 16~18개월을 보였지만, 환자 대부분이 내성을 갖는다.
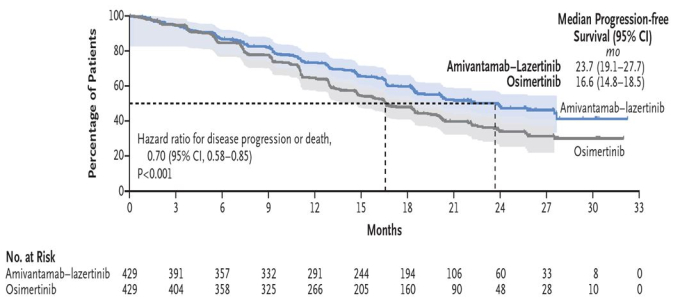
조 센터장 연구팀은 아미반타맙과 레이저티닙 병용 요법의 효과와 안전성을 확인했다. 병용요법 치료 환자 429명의 무진행생존기간, 반응지속기간은 각각 23.7개월, 25.8개월로, 오시머티닙 치료 환자(16.6개월, 16.8개월)보다 길었다. 2년 생존율도 병용군에서 74%로 나타나 오시머티닙군 69%보다 높았다. 병용 요법의 주요 부작용은 피부 발진과 손발톱 주변 염증 등으로 대개 조절이 가능한 상태였다.
조병철 센터장은 “이번 임상 결과를 바탕으로 FDA는 병용요법을 우선 심사 대상으로 선정했다”고 전했다. 레이저티닙과 아미반타맙 병용요법은 현재 FDA에 허가 신청된 상태로, 8월 중 결과가 나올 것으로 기대된다. 승인 완료 시 유한양행은 올해 4분기 중 얀센으로부터 6000만 달러(한화 약 826억원)의 마일스톤을 받게 된다.
박선혜 기자 betough@kukinews.com



































