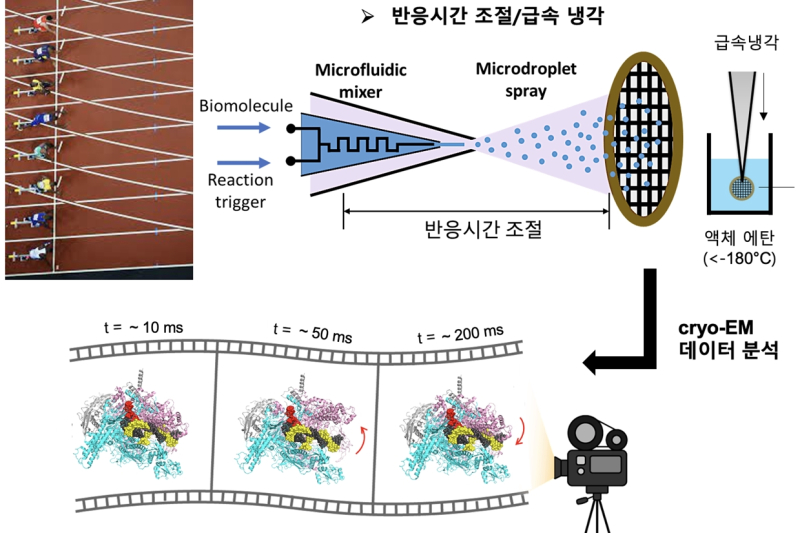
신약 개발은 순간적으로 일어나는 단백질의 동적 구조변화를 파악하는 것이 핵심이다.
단백질 복합체의 형성이나 분리는 ㎲~㎳ 수준의 극히 짧은 시간에 일어나며, 이는 단백질의 동적 구조변화에 의해 조절된다.
때문에 이 과정에서 생성되는 단백질 복합체의 중간상태 구조를 규명하는 것이 생명현상 이해에 매우 중요하다.
이를 연구하기 위해 단백질을 비결정질 얼음상태로 급속 냉각해 움직임을 멈추고 이미징하는 초저온전자현미경이 널리 사용되지만, 이는 시료를 냉각하는데 10초 이상이 소요돼 빠르게 변하는 단백질 복합체의 중간 상태를 포착하는 데 한계가 있었다.
이에 연구자들은 다양한 시간분해 초저온전자현미경(TRCEM) 기법을 개발했다. TRCEM은 단백질 복합체의 반응 중간상태를 초저온에서 빠르게 냉동해 구조를 분석할 수 있다.
하지만 이 역시 많은 시료 소비와 제한된 시간해상도 등의 한계로 어려움이 있었다.
단백질 반응순간 순간포착 성공
KAIST 화학과 강진영 교수와 물리학과 이원희 교수 공동 연구팀이 초고속 생화학반응 연구를 위한 ‘패릴렌(parylene) 기반 박막 미세유체 혼합-분사 장치’를 개발했다.
패릴렌은 단백질 반응을 초고속으로 관찰하기 위한 미세유체장치를 만드는 핵심 재료로, 수 ㎛의 얇은 박막형태로 스프레이 제작이 가능한 소재다.
이번 연구는 TRCEM 기법을 기존 대비 시료 소모량을 1/3 수준으로 줄이면서 분석 가능한 최소 반응시간은 6㎳(1000분의 6초)까지 단축한 것이 특징이다.
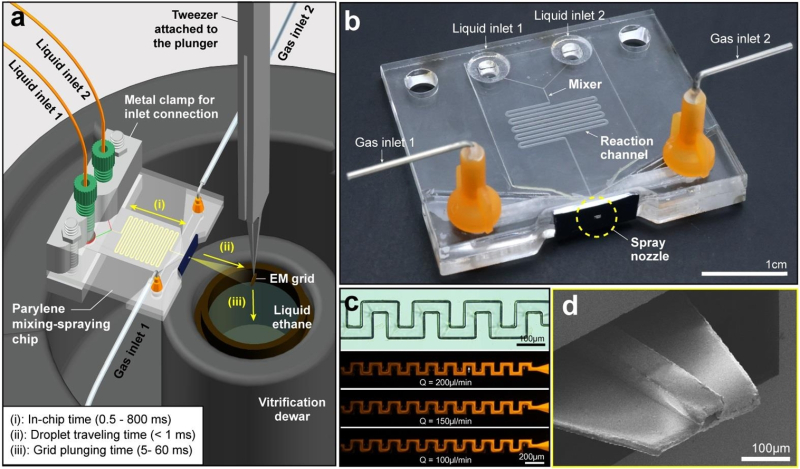
연구팀은 기존 TRCEM 기법의 시료 소비와 시간해상도 문제를 극복하기 위해 초박막 패릴렌 소재를 적용한 새로운 혼합분사장치를 개발했다.
이 장치는 시료의 양을 기존 대비 1/3 수준으로, 미세유체역학소자 내 반응 개시에 필요한 시료 혼합시간을 0.5㎳로 줄임으로써 해상도 6㎳를 달성했다.
아울러 연구팀은 소자의 일체형 설계로 실험 정밀도와 재현성도 높혔다.
강 교수는 “이번 연구는 단백질 상호작용 연구뿐 아니라 신약 개발, 효소반응 연구, 바이오센서 개발 등 다양한 생명과학 및 의약 분야에 폭넓게 활용될 것으로 기대한다”고 설명했다.
이번 연구는 KAIST 화학과 황혜랑 석박사통합과정이 제1저자로 수행했고, 연구결과는 국제학술지 ‘어드밴스드 펑셔널 머티리얼즈(Advanced Functional Materials)’ 지난 1월 28일 온라인에 게재됐다.
(논문명: Integrated Parylene-Based Thin-Film Microfluidic Device for Time-Resolved Cryo-Electron Microscopy, doi.org/10.1002/adfm.202418224).