mRNA는 단백질을 합성할 수 있는 DNA 유전정보를 세포질 내 리보솜에 전달하는 중간 매개체 역할 수행한다.
이를 응용한 mRNA 합성기법과 체내 전달물질인 지질나노입자 개발로 mRNA 치료제의 잠재력이 널리 인정받고 있다.
실제 지난 펜대믹에서 mRNA 기반 코로나19 백신이 널리 사용됐고, 향후 암이나 유전자 치료 등에도 활용이 가능해 성장 잠재력이 매우 크다.
하지만 mRNA 치료제가 세포 내에서 어떻게 조절되는지는 아직 충분히 연구되지 않은 상태다.
특히 코로나19 백신 ‘N1-메틸수도유리딘’ 변형 염기는 mRNA 백신의 효능 혁신과 상용화를 이끌었음에도 어떤 원리로 효능이 높아졌는지에 분명치 않았다.
mRNA 백신 작동원리 세계 최초 규명
기초과학연구원(IBS) 김빛내리 RNA연구단장 연구팀이 세계 최초로 mRNA 백신의 세포 내 전달과 분해를 제어하는 단백질군을 찾고 그 작동원리까지 규명했다.
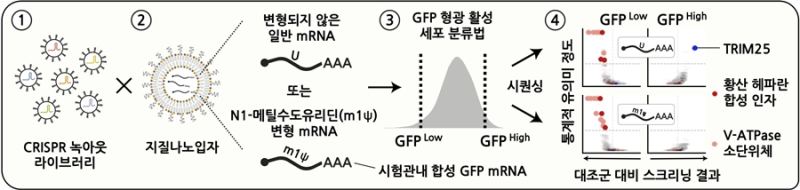
연구팀은 mRNA를 제어하는 세포 내 인자들을 찾아내고자 유전자가위를 이용한 녹아웃 스크리닝을 면밀히 진행했다. mRNA 치료제 효능을 높이고 부작용을 없애려면 mRNA가 세포로 유입・조절되는 인자와 활용되는 과정을 이해해야 가능하기 때문이다.
실험결과 mRNA가 세포 내로 전달・유입되는 데 필요한 핵심 단백질 인자들과 조절 경로를 밝혀냈다.
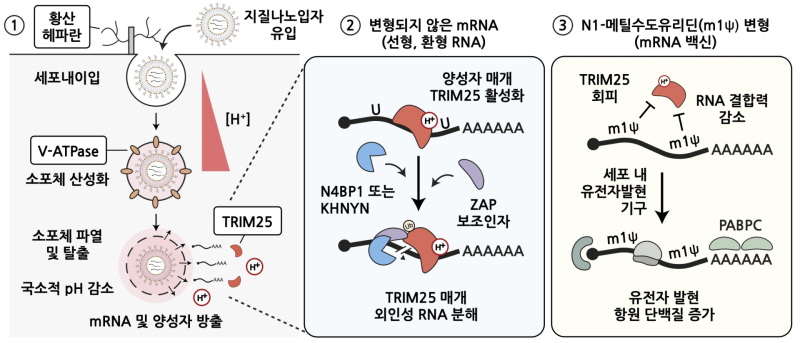
연구팀은 세포막 표면에 있는 ‘황산 헤파란’ 분자가 mRNA를 감싼 지질나노입자와 결합해 세포 내 유입을 촉진, 이를 통해 지질나노입자가 세포내 소포체로 들어가는 현상을 확인했다. 황산 헤파란은 세포 표면에 존재하는 황산화된 당단백질로, 병원체 감염과 나노입자의 세포 부착 등 외부 물질이 세포 내로 유입되는 데 중요한 매개체다.
이어 양성자 이온펌프 ‘V-ATPase’가 소포체 내부를 산성화시키고 지질나노입자가 양전하를 띄도록 해 소포체 막을 일시적으로 파열키면서 mRNA가 세포질로 방출, 단백질로 발현했다. V-ATPase는 V형 ATP 가수분해효소로, 양성자 이온을 소포 내부로 펌핑・산성화시키며. 산도를 조절해 세포 신호전달, 물질수송 등 다양한 과정을 지원한다.
특히 연구팀은 RNA 치료제에 대한 주요 억제인자와 함께 외부 RNA 침입을 경보하는 양성자이온의 중요한 역할도 최초로 발견했다.
세포질 내에서 바이러스 감염에 대한 선천성 반응을 조절하는 ‘TRIM25’ 단백질은 mRNA를 침입자로 인식하고 제거한다. 이 단백질은 소포체 막이 파열되면서 방출되는 양성자 이온에 의해 활성화되며, 외인성 RNA에 특이적으로 표적・결합해 다른 절단효소 및 보조 단백질과 함께 RNA를 빠르게 절단·분해한다.
아울러 연구팀은 mRNA를 결합・제거하는 TRIM25 단백질이 N1-메틸수도유리딘 변형 염기에는 그 결합력이 현저히 감소, mRNA를 절단・분해하지 못하는 것을 발견해 코로나19 mRNA 백신의 효능과 안정성을 향상시킬 수 있었던 요인과 원리를 규명했다.
이번 연구는 mRNA 백신의 세포 내 작동원리를 최초로 밝혀낸 것으로, mRNA 치료제의 효능과 안정성을 한 단계 높여갈 이론적 토대를 마련한 것으로 평가받는다.
김 단장은 “이번 연구는 최초로 양성자이온의 역할은 규명함으로써 향후 RNA 면역반응 연구에 도움을 줄 것으로 기대된다”며 “향후 TRIM25가 선호하는 RNA의 특징을 이해하고 TRIM25가 외인성 mRNA를 인지하는 원리를 구체적으로 밝혀 안정적으로 작동하는 RNA 치료제를 개발에 중요한 역할을 할 것”이라고 설명했다.
한편, 이번 연구는 김명환 IBSRNA연구단 연구원이 제1저자로 참여했고, 연구결과는 국제학술지 사이언스(Science, IF 44.7)‘ 4일자 온라인에 게재됐다.






























