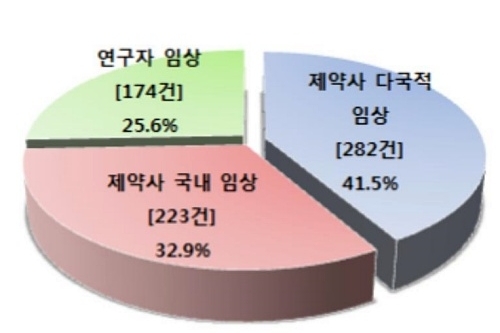
 식품의약품안전처가 ‘18년 임상시험계획 승인 현황을 분석한 결과, 전체 승인건수는 679건으로 ‘17년(658건) 대비 3.2% 증가하는 등 임상시험 승인건수 증가세가 지속되고 있는 것으로 나타났다.
식품의약품안전처가 ‘18년 임상시험계획 승인 현황을 분석한 결과, 전체 승인건수는 679건으로 ‘17년(658건) 대비 3.2% 증가하는 등 임상시험 승인건수 증가세가 지속되고 있는 것으로 나타났다. 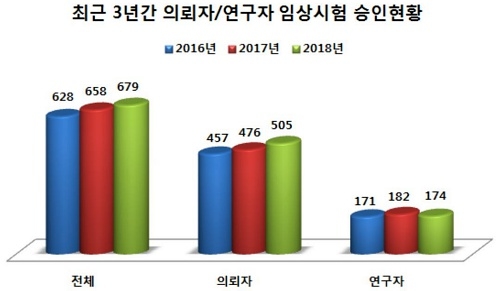
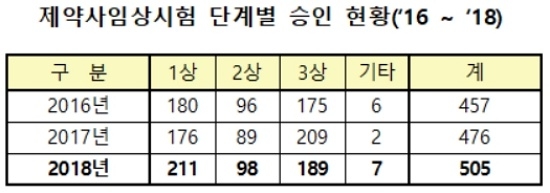
조민규 기자 kioo@kukinews.com
 식품의약품안전처가 ‘18년 임상시험계획 승인 현황을 분석한 결과, 전체 승인건수는 679건으로 ‘17년(658건) 대비 3.2% 증가하는 등 임상시험 승인건수 증가세가 지속되고 있는 것으로 나타났다.
식품의약품안전처가 ‘18년 임상시험계획 승인 현황을 분석한 결과, 전체 승인건수는 679건으로 ‘17년(658건) 대비 3.2% 증가하는 등 임상시험 승인건수 증가세가 지속되고 있는 것으로 나타났다. 

조민규 기자 kioo@kukinews.com
국민의힘이 더불어민주당을 오차범위 밖에서 앞섰다는 여론조사 결과가 나왔다. 22일 조원씨앤아이가 스트레이
12·3 비상계엄 사태에 따른 탄핵 정국이 장기화되며 국민의힘 지지율이 더불어민주당을 오차범위 밖에서 앞
12·3 비상계엄 사태의 진상 규명을 위한 국회 국정조사 특별위원회는 첫 청문회에 불출석한 윤석열 대통령,
법원이 윤석열 대통령 구속영장 발부에 반발해 서울서부지법에 침입한 56명에 대해 구속영장이 발부했다. 22일
6명의 사망자가 발생한 광주 화정 아이파크 붕괴 사고 관련 시공사 HDC현대산업개발 당시 경영진들이 무죄 판결을
중앙선거관리위원회(선관위)가 윤석열 대통령이 국회의 탄핵소추 후 지지율 40%를 기록했다는 한국여론평판연구
권영세 국민의힘 비상대책위원장이 당원들에게 ‘겸손한 자세’와 ‘신중한 언행’을 당부했다.
경기도 고양시에서 독도홍보관을 운영하고 있는 ㈔영토지킴이독도사랑회가 필리핀에서 ‘독도는 한국땅&rsquo
국회 ‘내란 혐의 진상 규명 국정조사 특별위원회’가 22일 첫 청문회를 열었다. 다만 윤석열 대통령을 비
트럼프 대통령 취임식 참석차 미국을 방문 중인 국민의힘 김대식 의원(부산 사상구)은 미국 워싱턴 D.C.에서 테드
SNT다이내믹스가 포항공과대학교(POSTECH)와 산학협력 협약을 체결했다. 21일 SNT다이내믹스 본사에서 열린 산학협
홍원식 전 남양유업 회장이 ‘이사 보수한도 셀프 결의’와 관련해 1심에 이어 2심에서도 패소했다. 서울
수서고속철도(SRT) 운영사 에스알(SR)은 설 명절 기간 SRT 운임을 최대 40%까지 할인하는 ‘알뜰 승차권’을 판



